Helseøkonomisk evaluering
Publisert
Dette delkapittelet belyser hvorfor vi gjør helseøkonomiske evalueringer og hvordan vi vanligvis gjør dette.
Dette delkapittelet er todelt. I første del belyser vi bakgrunnen for å gjøre helseøkonomiske evalueringer og skisserer ulike analysetyper. I andre del beskriver vi hvordan vi gjør modellbaserte helseøkonomiske evalueringer ved FHI. Her trekker vi frem hovedpunkter fra retningslinjen for levering av dokumentasjon for hurtig metodevurdering av medisinsk utstyr og diagnostikk, og refererer til den for mer detaljerte beskrivelser (1).
Hva er helseøkonomiske evalueringer og hvorfor gjør vi dem?
Helsesektoren må forholde seg til begrensede ressurser og gitte budsjetter. Hensikten med helseøkonomiske evalueringer er å gi bedre informasjonsgrunnlag for beslutninger som bidrar til mest mulig effektiv bruk av helsesektorens ressurser, i tråd med nasjonale retningslinjer for prioritering (2). Kjernen i en helseøkonomisk evaluering er å sammenligne kostnader og helseeffekter ved ulike tiltak.
I Norge er slike beslutninger (om innføring, bruk eller utfasing av metoder) basert på tre prioriteringskriterier: nytte, ressursbruk og alvorlighet (2). Skjønnsmessige vurderinger skal også inngå i totalvurderinger av tiltak på gruppenivå, som for eksempel etiske aspekter. Prioriteringskriteriene skal vurderes samlet og veies mot hverandre. Jo større nytte et tiltak har og jo mer alvorlig en tilstand er, jo høyere ressursbruk kan aksepteres (2).
- Nytte: «Et tiltaks prioritet øker i tråd med den forventede nytten av tiltaket» (2). Nytten defineres som økt livslengde og/eller livskvalitet. Den skal måles i antall gode leveår (kvalitetsjusterte leveår; QALYs) i metodevurderinger.
- Ressursbruk: «Et tiltaks prioritet øker desto mindre ressurser det legger beslag på» (2). Når vi innfører tiltak trengs det personell, utstyr, fasiliteter osv. som alternativt ville blitt brukt på andre pasienter om ikke tiltaket hadde blitt innført. Dette omtaler vi som alternativkostnaden av tiltaket. Jo mer ressurser som brukes til et tiltak for én pasientgruppe, jo mindre ressurser er tilgjengelig for andre.
- Alvorlighet: «Et tiltaks prioritet øker i tråd med alvorligheten av tilstanden» (2). Alvorlighet måles som absolutt prognosetap og dette er tap av fremtidige gode leveår uten tiltaket som vurderes, altså med dagens behandling. For forebyggende tiltak skal alvorlighet beregnes for pasientgruppen som hadde fått sykdommen uten tiltaket, altså med dagens behandling.
Kort om kostnadseffektivitet
Prioriteringskriteriene skal vurderes samlet og veies mot hverandre. Ved å sammenstille de første to kriteriene, får vi fram hvor stor nytte (QALYs) ressursene kan forventes å oppnå. Ved spørsmål om innføring av nye metoder er det vanligvis en situasjon hvor den nye metoden har høyere nytte/effekt og samtidig høyere ressursbruk/kostnader. Vi beregner derfor forholdet mellom kostnad og helseeffekt i en inkrementell analyse hvor forskjell i kostnad sammenlignes med forskjell i helseeffekter for hvert av tiltakene. Dette uttrykker hvor mye ekstra et tiltak koster for å oppnå én ekstra effektenhet i forhold til et annet tiltak, altså kostnad per vunnet effektenhet (ofte i form av QALY). Dette uttrykker vi typisk som en inkrementell kostnad-effekt-ratio (incremental cost-effectiveness ratio, ICER), også kalt kostnad-effektbrøk:
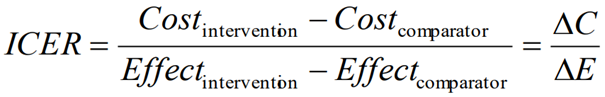
Analyseperspektiv og estimering av kostnader
Analyseperspektivet avgjør hvilke kostnader og nyttevirkninger som skal inkluderes i analysen. I helseøkonomiske evalueringer er helsetjenesteperspektivet og samfunnsperspektivet de vanligste. I et helsetjenesteperspektiv inkluderes kostnader og konsekvenser innen helsetjenesten, mens i et samfunnsperspektiv skal alle kostnader og konsekvenser som påløper pasienter og andre relevante aktører tas med. Dette kan for eksempel være potensielle endringer i produksjonstap (tapt verdiskapning som for eksempel ved sykefravær på grunn av sykdom) som følge av innføring av et nytt tiltak (4).
For metodevurderinger som støtter beslutninger om prioritering i helsesektoren bruker vi et såkalt «utvidet helsetjenesteperspektiv». Her er det i hovedsak helsesektorens ressursbruk som tas hensyn til, men i tillegg vil man kunne inkludere relevante kostnader utenfor helsetjenesten så lenge det ikke gir urettferdige fordelingsvirkninger (2).
Ulike analyser
For å beregne forholdet mellom kostnad og helseeffekt er ulike metoder aktuelle (5).
Kostnad per QALY-analyse (cost-utility analysis, CUA)
Den anbefalte analysen for å støtte beslutninger om prioriteringer av metoder på gruppenivå i Norge, er kostnad per QALY-analyse. Et kvalitetsjustert leveår (QALY) fanger opp både vunnet leveår og forbedret helse som følge av behandling. Ved å bruke et slikt generisk utfallsmål kan vi sammenligne kostnadseffektivitet på tvers av sykdomsområder.
Generelt, når effekten av et tiltak uttrykkes i en ikke-monetær enhet, omtales slike analyser som kostnad-effekt analyser (cost-effectiveness analysis, CEA). I helseøkonomisk litteratur brukes ofte begrepet cost-utility analysis (CUA) for en undergruppe av CEA som beregner effekter i en generisk preferansebasert enhet, slik som QALYs.
Kostnadseffektivitetsanalyse (cost-effectiveness analysis, CEA)
Hvis effektmålet er klinisk effekt alene beregner vi kostnad per klinisk effektenhet, for eksempel vunnet leveår, redusert sykelighet, symptomreduksjon eller unngåtte hendelser (for eksempel hoftebrudd). Kostnadseffektivitetsanalyser kan være nyttige for å sammenligne alternative tiltak innenfor et terapiområde. Men, denne typen analyse kan i hovedsak ikke brukes for å sammenligne og prioritere på tvers av sykdomsområder.
Kostnadsminimeringsanalyse (cost-minimisation analysis, CMA)
Det kan være tilfeller hvor det vil være tilstrekkelig med mindre omfattende helseøkonomiske analyser. Hvis effektdokumentasjonen viser at resultater for effekt og sikkerhet er faglig likeverdige for tiltaket og sammenligningene, kan en kostnadsminimeringsanalyse være aktuell. Her sammenlignes kostnadene ved de ulike metodene, som oppnår samme helseeffekt. Det er imidlertid begrensninger ved denne typen analyse fordi det er knyttet usikkerhet til estimater for effekt og kostnader, og det er ofte problematisk å konkludere med at tiltakene faktisk er likeverdige når det kommer til helseeffekt (5).
Kostnad-nytteanalyse (cost-benefit analysis, CBA)
I kostnad-nytteanalyser (cost-benefit analysis, CBA) verdsettes tiltakets nytte/effekt i penger, til forskjell fra CEA og CUA der nytte/effekt uttrykkes i helseenheter. Med nytte menes samfunnets betalingsvillighet (i kroner) for å ha et helsetjenestetilbud tilgjengelig. Denne typen analyser benytter vi vanligvis ikke for metodevurdering av helsetiltak i Norge. Dette er blant annet fordi i slike analyser skal helseeffekter verdsettes i monetære verdier, og Prioriteringsmeldingen legger ikke opp til denne typen analyser (2).
Kostnad-konsekvensanalyse (cost-consequence analysis)
Kostnad-konsekvensanalyse er en form for helseøkonomisk evaluering der alle kostnader, samt en liste over forskjellige utfall, er presentert separat for hvert av behandlingsalternativene. Denne metoden er lite benyttet for vurdering av helsetiltak i Norge, men kan være et alternativ ved veldig begrenset datagrunnlag eller når de ulike utfallsmålene ikke lar seg aggregere som QALYs.
Anvendelse av helseøkonomisk evaluering ved FHI
Hvor mye tid og ressurser vi setter av til å gjøre en økonomisk evaluering, avhenger blant annet av hvor godt dokumentert effekten er, hva som er problemstillingen, hva som har vært gjort tidligere av denne typen analyser på det aktuelle feltet, samt kompleksiteten ved den beslutningsanalytiske modelleringen. Vi gjør enklere analyser der vi mener det er hensiktsmessig og/eller dersom det er spesifisert i oppdraget. Enklere analyser kan fungere som bestillingsstøtte til mer omfattende oppdrag. For hvert oppdrag gjør vi en vurdering av hvilken type analyse vi skal gjøre.
Vi etterstreber å basere de helseøkonomiske analysene på beste tilgjengelig informasjon om kostnader og effekter. Vi samarbeider tett med kliniske eksperter for å få informasjon om ressursbruk og klinisk praksis i Norge, og deretter beregner vi kostnader basert på tilgjengelige kostnadskilder slik at dette skal reflektere norsk behandlingspraksis. Innspill fra ekspertene er også viktig ved utarbeidelse av modell, med tanke på relevante kliniske utfall, alvorlige hendelser/komplikasjoner, sykdomsforløp og behandlingsforløp.
I størst mulig grad baserer vi oss på dokumentasjonen fra vurderingen av effekt og sikkerhet i metodevurderingen. Vi er i tillegg avhengig av nyttevekter for helserelatert livskvalitet når vi skal beregne QALYs.
Helseøkonomisk evaluering av tiltak kan gjøres som en del av kliniske effektstudier, eller ved bruk av modell, eller som en kombinasjon av de to. Vanligvis gjør vi modellbaserte helseøkonomiske evalueringer. Basert på tilgjengelige datakilder for kostnader, norsk praksis, nytte og risiko for ulike hendelser, lager vi en modell som brukes til å beregne forholdet mellom kostnad og effekt. En fordel med modellbaserte analyser er at vi kan beregne resultater over et lengre tidsrom, ofte for pasientgruppens forventede levetid. I tillegg kan vi med modellbaserte analyser gjøre usikkerhetsanalyser for å kartlegge hvordan resultatet påvirkes av endringer i forutsetningene vi gjør i modellen. Dette gjør vi med sensitivitets- og scenarioanalyser for å se hvordan resultatet (f.eks. kostnad-effektforholdet) påvirkes av variasjoner og/eller endringer i premissene som legges til grunn for analysen. Med dette kan vi også se hvilke parametere som er mest usikre, og belyse verdien av ny informasjon gjennom ytterligere studier. Dette kan gi beslutningstakere, på et transparent grunnlag, informasjon om beslutningen bør avventes til ny informasjon som kan redusere usikkerheten er tilgjengelig. Modellen kan også være aktuell for å benyttes i andre land eller kontekster (med lokale tilpasninger).
Fremgangsmåte for modellbasert helseøkonomisk evaluering
Beskrivelse av sykdomsområde, pasientpopulasjon, tiltak og sammenligning
For den helseøkonomiske analysen må vi identifisere den eller de mest relevante sammenligningene for norsk klinisk praksis. Dette er vanligvis tiltakene som sannsynligvis blir erstattet helt eller delvis av det nye tiltaket (dagens behandling). For å sikre at vi har inkludert de viktigste sammenligningene er vi avhengige av innspill fra fagekspertene i prosjektgruppen.
Sykdomsområdet, epidemiologi, pasientpopulasjon, tiltak og sammenligning er som regel beskrevet i begynnelsen i metodevurderingen. Pasientpopulasjonen i den helseøkonomiske analysen kan imidlertid i enkelte tilfeller være forskjellig for å være relevant for Norge. Hvis det er forskjeller i populasjon og/eller sammenligninger (komparatorbehandling) mellom effektdelen og den helseøkonomiske evalueringen bør dette beskrives og begrunnes. Hvis vi gjør analyser for delpopulasjoner, redegjør vi for dette.
Analysemetode, tidshorisont og analyseperspektiv
Den anbefalte analysen for helseøkonomisk evaluering er kostnadseffektivitetsanalyse med kvalitetsjusterte leveår som effektmål. Tidshorisonten skal være lang nok til å fange opp alle fremtidige forskjeller i kostnader og helseeffekter mellom tiltakene. I økonomiske evalueringer for spesialisthelsetjenesten skal analyseperspektivet være et «utvidet helsetjenesteperspektiv». Se kapittel 9 i retningslinjene for beskrivelse av hva som skal inkluderes (1).
Kvalitetsjusterte leveår og helserelatert livskvalitet
For å beregne kvalitetsjusterte leveår trenger vi livskvalitetsdata i form av nyttevekter (health state utility weights), som er tall mellom 0 og 1, hvor 1 er perfekt helse. Vi kan finne nyttevekter direkte i kliniske studier for relativ effekt, men dersom studien(e) ikke har brukt relevante instrumenter (f.eks. EQ-5D) for å måle helserelatert livskvalitet som nyttevekter, bør vi søke i databaser som har samlet informasjon om nyttevekter eller søke etter andre kostnad per QALY-analyser (CUA) som har sett på samme behandling. Hvis nyttevekter fra annen litteratur (enn de kliniske studiene) brukes, bør vi dokumentere hvordan søket ble utført. Hvis det ikke finnes data fra generiske instrumenter, kan data fra sykdomsspesifikke verktøy konverteres til EQ-5D-verdier med bruk av algoritme. Se kapittel 8 i retningslinjene for mer informasjon (1).
Hva er EQ-5D?
EuroQol five-dimensional (EQ-5D) er et spørreskjema som omfatter spørsmål i fem områder. Hvert område har tre eller fem nivåer for å indikere grad av problemer med gange, personlig stell, vanlige gjøremål, grad av smerte/ubehag, og grad av angst/depresjon (6).
I en modell estimeres QALYs ved å multiplisere nyttevekter med tidsperioder i gitte helsetilstander. Her kan vi også vekte for (midlertidig) redusert livskvalitet som følge av uønskede hendelser (for eksempel komplikasjoner, bivirkninger og skade).
Det kan også være aktuelt å belyse hvordan metoden eventuelt påvirker de pårørendes helserelaterte livskvalitet og hvordan dette kan påvirke resultatet.
Se kapittel 8 i retningslinjene for mer informasjon om helserelatert livskvalitet og nyttevekter (1).
Modellering
I helseøkonomiske modeller sammenfatter vi data fra ulike kilder for å kunne si noe om hva som skjer hvis vi innfører det aktuelle tiltaket, sammenlignet med dagens praksis. Vi bruker modeller fordi med dem kan vi sammenligne tiltak som det ikke er mulig å undersøke i randomiserte kontrollerte forsøk, og vi kan inkludere flere aspekter. Randomiserte kontrollerte forsøk har også ofte for kort oppfølgingstid til å fange opp alle relevante effekter, og det kan hende de ikke rapporterer det utfallet vi er interesserte i når vi gjør økonomisk evaluering. Vi lager beslutningsmodeller som er beslutningstre, Markov-modell, eller andre oppsett som er nødvendige. Ved analyser av sykdommer/tilstander hvor pasienter er uavhengige av hverandre (helsen til et individ påvirker ikke et annet) brukes statiske modeller. Imidlertid, ved analyser av infeksjonssykdommer er det ofte nødvendig med en dynamisk modellstruktur for å reflektere sykdomsoverføring. Det er fordi denne modellstrukturen tar hensyn til endringen i risiko for infeksjon mellom vaksinerte og uvaksinerte individer, samt redegjør for både direkte og indirekte effekter av vaksinasjon (8). For mer informasjon om modellering av infeksjonssykdommer, se bl.a. Direktoratet for medisinske produkters retningsgivende notat om dokumentasjonsgrunnlag for hurtig metodevurdering av vaksiner (3).
Modeller har en struktur (oppsett), antakelser og inndata. Resultatene fra en modell er helseeffekter og kostnader som summeres opp for hele tidsperioden slik at de kan sammenlignes mellom tiltakene. Modeller er nyttige som beslutningsstøtte, men vil alltid være forenklinger av virkeligheten.
Når vi bestemmer modellens struktur, må vi tenke på hvilke hendelser eller tilstander vi skal undersøke. Det er viktig å vite mye om sykdommen man skal modellere, hva som er dagens behandlingspraksis og hvordan et typisk pasientforløp ser ut. Dette får vi hjelp til av fagekspertene i prosjektet. Vi tar ikke med alt, men bør ha med det som har størst innvirkning på kostnader og pasientutfall og som har betydning for forskjellen mellom tiltakene som sammenlignes (9).
Inndata omfatter:
- Kliniske effektdata: Disse tas vanligvis fra oppsummeringen av effekt i metodevurderingen. Ofte må vi ekstrapolere effektdata utover studieperioden. Se kapittel 6 i retningslinjene for mer informasjon om dette (1).
- Epidemiologiske data: Dette er bakgrunnsrisiko for befolkningen som brukes til å modellere hva som skjer med pasientene. Dette kombineres med den relative effekten fra effektdelen for å få sannsynligheten for overgang mellom tilstander.
- Kostnader: Vi må ha enhetskostnader som er basert på norske markedspriser og ressursbruk i norsk klinisk praksis. Vi må også ha med kostnader for å behandle uønskede hendelser i modellen. Se kapittel 9 i retningslinjene for informasjon om ressursbruk og kostnader (1).
- Nyttevekter: Vi anvender nyttevekter for helsetilstander i modellen og for hendelser som gir redusert (eller økt) livskvalitet.
Kilder for disse inndataene kan være resultater fra den systematiske oversikten i metodevurderingen (bl.a. helseeffekter og overgangssannsynligheter), randomiserte kliniske forsøk, observasjonelle studier, administrative databaser, sykdomsregistre, offisielle nettsider eller dokumenter med takster og tariffer, og innspill fra fageksperter. Publiserte helseøkonomiske analyser/metodevurderinger, livskvalitetsstudier, epidemiologiske oppsummeringer, og upubliserte data fra leverandører/produsenter kan også være aktuelle kilder (7).
Dersom det finnes relevante utenlandske modeller av høy kvalitet for økonomisk evaluering, kan det være aktuelt å «låne» og tilpasse en utenlandsk modell (for norsk kontekst), og lage beregninger basert på norsk praksis og kostnadstall, samt norske epidemiologiske data. Ofte erstatter vi effektestimater fra oppsummeringen av effekt i vår metodevurdering. Andre parametere, bl.a. nyttevekter, og de inkluderte hendelsene/komplikasjoner kan også oppdateres.
Beregning av alvorlighet
Kostnad-effektbrøken (ICER), altså kostnad per vunnet kvalitetsjusterte leveår, skal vurderes opp mot sykdommens eller tilstandens alvorlighet (2). I metodevurderinger kvantifiseres alvorlighet som absolutt prognosetap. Absolutt prognosetap er antall framtidige gode leveår en gjennomsnittspasient i en pasientgruppe mister på grunn av sykdommen sammenlignet med gjennomsnittet i befolkningen med samme alder. Absolutt prognosetap er det samme som tap av forventede fremtidige gode leveår uten den behandlingen som vurderes, det vil si med dagens standardbehandling. For beskrivelse av hvordan vi beregner absolutt prognosetap, se kapittel 11 i retningslinjene (1).
Usikkerhet
Det vil som regel være usikkerhet knyttet til blant annet inndataene, antakelsene bak og strukturen i modellen og vi utforsker dette med sensitivitets- og scenarioanalyser. Effekten av heterogenitet blant pasienter bør undersøkes med subgruppeanalyser. Disse bør defineres i samråd med kliniske fageksperter og spesifiseres i prosjektplanen.
Deterministiske sensitivitetsanalyser gjøres som enveis, toveis og/eller terskel- og scenarioanalyser. Enveisanalyser varierer parametere en og en for å undersøke deres påvirkning på resultatet (kostnad-effektforholdet). Dette vises ofte som et tornadodiagram som illustrerer parametere etter størst påvirkning på resultatet. Vi kan også gjøre terskelanalyse (som en variant av enveisanalysen) som viser «vippepunktet» for en parameter eller kombinasjon av parametere, altså ved hvilken verdi parameteren(e) vil endre beslutningen basert på resultatet. I to- og flerveis sensitivitetsanalyse blir flere parametere variert samtidig (5).
I scenarioanalyser illustreres et utvalg av flerveis sensitivitetsanalysene. Dette vil ofte være et grunnscenario (base case), optimistisk og pessimistisk scenario, eller andre scenarioer vi mener er relevante.
Deterministiske sensitivitetsanalyser kan brukes bl.a. for å vise kostnad-effektforholdet ved ulike priser, dette kan være nyttig ved eventuelle forhandlinger om pris. Men slike analyser alene er ikke tilstrekkelig for å håndtere parameterusikkerhet, og bør suppleres med probabilistiske analyser.
I probabilistiske sensitivitetsanalyser kan vi undersøke alle parameternes usikkerhet samtidig. Her angir vi (ulike) sannsynlighetsfordelinger for modellparameterne som gjør det mulig å erstatte «faste» parameterverdier med verdier som tilfeldig trekkes fra fordelingene. Når vi gjør dette x antall ganger kan vi estimere kostnad-effektforhold for hver av disse trekningene. Dette viser vi gjerne som spredningsdiagram (scatter plot) av kostnad-effektforholdene ved alle simuleringene, i tillegg til kostnadseffektivitets-akseptabilitetskurve (cost-effectiveness acceptability curve, CEAC), eller kostnadseffektivitets akseptabilitetsgrenser (cost-effectiveness acceptability frontier, CEAF). Dette viser sannsynligheten for at metoden faktisk er kostnadseffektiv ved ulike terskler for betalingsvillighet (5). Disse simuleringene fra den probabilistiske sensitivitetsanalysen kan også brukes til å gjøre analyser av den forventede verdien av informasjon. I slike analyser vises den monetære kostnaden ved en eventuell feil beslutning. Dette gjør vi fordi det er knyttet usikkerhet til resultatet og dermed er det en risiko for at det faktiske mest kostnadseffektive tiltaket ikke velges, og dette har konsekvenser. Resultatene av en analyse av forventet verdi av perfekt informasjon (expected value of perfect information, EVPI) brukes til å undersøke verdien av å drive mer forskning fremfor å treffe en beslutning umiddelbart. En variant av denne analysen er en delvis EVPI (expected value of partial perfect information, EVPPI). Denne viser hvor mye av usikkerheten som er grunnet spesifikke parametere og angir verdien av å fjerne denne usikkerheten. Dermed kan forskning rettes konkret mot den enkelte parameteren (5).
Se kapittel 12 i retningslinjene for mer informasjon om de ulike usikkerhetsanalysene (1).
Budsjettkonsekvenser
Budsjettkonsekvensanalyser brukes for å anslå mulige endringer i fremtidige utgifter hvis det nye tiltaket innføres og fortrenger helt eller delvis eksisterende tilbud. Vi beregner vanligvis for fem år frem i tid og på nasjonalt nivå. To scenarier blir vanligvis beregnet for: et hvor det nye tiltaket innføres og ett med dagens tilbud. Budsjettkonsekvensen er differansen mellom scenariene. Se kapittel 13 i retningslinjene for beskrivelse av hvordan dette beregnes (1).
Helseøkonomiske evalueringer basert på publiserte analyser eller andres modeller
Helseøkonomiske evalueringer er i mindre grad overførbare mellom land/kontekster enn effektstudier, siden klinisk praksis, kostnader, risiko og forekomst for ulike hendelser varierer mellom land, og at helsetjenesten er organisert forskjellig. I noen tilfeller kan det være aktuelt å ta utgangspunkt i tidligere publiserte helseøkonomiske studier og tilpasse til norske forhold. For eksempel kan helseøkonomiske beslutningsmodeller være nyttige på tvers av land og kontekster med tilpasset informasjon om for eksempel ressursbruk epidemiologiske data (7).
Det finnes flere sjekklister og retningslinjer for vurdering av helseøkonomiske studier, eksempelvis:
- Drummond et al. sin sjekkliste for vurdering av økonomiske evalueringer (https://www.nlm.nih.gov/nichsr/edu/healthecon/drummond_list.html) (4)
- CHEERS-sjekklisten, Consolidated Health Economic Evaluation Reporting Standards (10)
- EUnetHTAs retningslinje om praktiske hensyn ved kritisk vurdering av økonomiske evalueringer (11)
- Anbefalinger fra en arbeidsgruppe i ISPOR (The Professional Society for Health Economics and Outcomes Research) for kritisk vurdering av systematiske oversikter med kostnader og kostnadseffektivitet (12)
Viktige elementer i arbeidet med helseøkonomisk evaluering i en metodevurdering
Helseøkonomiske evalueringer gjennomføres parallelt med oppsummeringen av effekt og sikkerhet. Dersom metodevurderingen har et eget kapittel med beskrivelse av organisering, bør dette samordnes med den helseøkonomiske evalueringen da det kan være overlapp for eksempel angående beskrivelse av organisering av tiltaket, ressursbruk, og investeringer som er nødvendige. Det er viktig at helseøkonomer er med fra start. Samarbeidet mellom det øvrige laget og helseøkonomene er viktig for å sikre at relevant informasjon blir gjort tilgjengelig i riktig format for den helseøkonomiske analysen. Vi skisserer her betydningsfulle elementer i dette arbeidet. Disse punktene kan foregå trinnvis, men også parallelt:
- I alle metodevurderinger vurderer vi behovet for en helseøkonomisk evaluering. Dersom oppdraget ikke inneholder en helseøkonomisk analyse bør dette ha blitt diskutert med en helseøkonom, og vurderingen bør ha blitt gjort med hensyn til prioriteringskriteriene. Vi bør redegjøre i den endelige rapporten om hvorfor en helseøkonomisk analyse ikke er med.
- Helseøkonomer (og ev. statistiker) bør tidlig avtale med laget om når og hva slags data som trengs fra effektdelen for å starte med sine analyser.
- Helseøkonomene tar stilling til hva slags analyse de skal utføre basert på (utkast til) resultater for effekt. Det kan eventuelt være nødvendig med GRADE-resultater for å ta denne beslutningen. Hvis ikke, bør helseøkonomene få effektresultater før GRADE-vurderingene starter.
- Helseøkonomene avtaler med bibliotekar dersom det skal utføres et søk etter helseøkonomiske studier (og eventuelt nyttevekter). Det er viktig at helseøkonomer og bibliotekarer avklarer de forskjellige aspektene ved søket (bruk av søkefiltre, valg av databaser, aktuelle søketermer og -strategier).
- Helseøkonomene diskuterer med fagekspertene for å få en god forståelse av sykdomsforløp, faser under behandling og eventuelt alvorlige hendelser, osv., samt begynner å skissere modellen (dette kan eventuelt være en tilpasning av tidligere publisert modell).
- Vi innhenter all informasjonen vi trenger til analysen, i tillegg til effektdata fra oppsummeringen. Dette vil være bl.a. kostnader, nyttevekter og epidemiologiske data. Deretter ferdigstiller vi den helseøkonomiske modellen.
- Modellen benyttes til å svare på prioriteringskriteriene ved å utføre kostnadseffektivitetsanalyser, usikkerhetsanalyser og eventuelle budsjettkonsekvensanalyser og analyse av absolutt prognosetap (alvorlighet).
- Rapporten skrives (sammen med det øvrige laget). Vi får utført fagfellevurdering av den helseøkonomiske evalueringen, enten av en ekstern eller intern fagfelle (hvis modellbasert analyse, gjerne både intern og ekstern fagfelle).
Kilder
Flere av delkapitlene i kapittelet om metodevurdering er i hovedsak basert på EUnetHTA HTA Core Model ® (7). HTA Core Model ®-domenet om kostnader og økonomisk evaluering har som mål å fremme transparens og systematikk i rapportering av informasjonen som brukes i en helseøkonomisk evaluering. Domenet om kostnader og økonomisk evaluering er ikke ment for å harmonisere metoder for å utføre helseøkonomiske evalueringer. Derfor har vi brukt domenet i HTA Core Model ® i liten grad her, men hovedsakelig basert dette delkapittelet på retningslinjen for levering av dokumentasjon for hurtig metodevurdering av medisinsk utstyr og diagnostikk (1).